Вихревые модели атомов кислорода
У кислорода стабильными являются изотопы O16, O17 и O18. Рассмотрим несколько теоретически наиболее возможных конфигураций атомов этих изотопов. Каждая конфигурация сопровождается соответствующей формулой современного математического описания.

Рисунок 1. Вероятные конфигурации атомов кислорода
Соответствующие этим атомам ядра изображены на рисунке ниже. Овалом обведены протоны, вращающиеся вокруг нейтронной оси. Экспериментальному значению основного состояния спина ядра O16(0) соответствуют первая и седьмая конфигурации. Обе комбинации химически инертны, то есть в любом случае данный изотоп в основном состоянии не может вступать в химические реакции. Главным претендентом на основное состояние является седьмая конфигурация, потому что она более компактна и содержит более крепкое ядро (с двумя альфа-частицами). Экспериментальному значению основного состояния спина ядра O17(5/2) соответствуют третья и четвертая конфигурации. Главным претендентом на основное состояние является четвертая конфигурация, потому что она более компактна и содержит более крепкое ядро (с одной альфа-частицей). Данная конфигурация является химически агрессивной.
Экспериментальному значению основного состояния спина ядра O18(0) соответствует только одна химически инертная седьмая конфигурация. Современному математическому описанию данного атома полностью соответствует количественный состав электронных слоев шестой и седьмой конфигурации.

Рисунок 2. Ядра атомов кислорода
Химические свойства атома кислорода второй конфигурации должны быть идентичны химическим свойствам осевого атома гелия, атома фтора с осевым лепестком, атома лития второй конфигурации. Химические свойства атома кислорода четвертой конфигурации должны быть идентичны химическим свойствам атома фтора с электронной вакансией в боку, атома бора седьмой конфигурации. Только эта конфигурация подходит в качестве модели атома кислорода в молекуле углекислого газа. Расчетное значение угла между валентными связями равно 180 градусов. Экспериментальные измерения – угол между валентными связями равен 180 градусов, а расстояние между ядрами атомов кислорода и водорода равно 1,16 ангстрем – меньше, чем обычно для связи C-O (1.23 ангстрема).
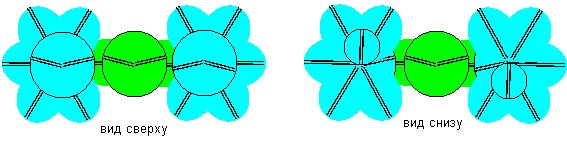
Рисунок 3. Модель молекулы углекислого газа
Химические свойства атома кислорода пятой конфигурации должны быть идентичны химическим свойствам атома углерода первой конфигурации. Химические свойства атома кислорода шестой конфигурации должны быть идентичны химическим свойствам атома углерода пятой конфигурации. Только эта конфигурация подходит в качестве модели атома кислорода в молекуле воды. Расчетное значение угла между валентными связями равно 109, 5 градусов. Экспериментальные измерения – угол между валентными связями равен 104,5 градуса, а расстояние между ядрами атомов кислорода и водорода равно 0,96 ангстрем.
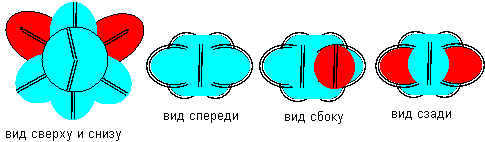
Рисунок 4. Модель молекулы воды
Химические свойства третьей конфигурации еще не рассматривались ранее. Она способна образовывать две нейтральные валентные связи на противоположных полюсах атома. На рисунке ниже показаны способы взаимодействия атомов третьей конфигурации с атомами лития, гелия, водорода и фтора особых конфигураций, имеющих нейтральную валентную связь.
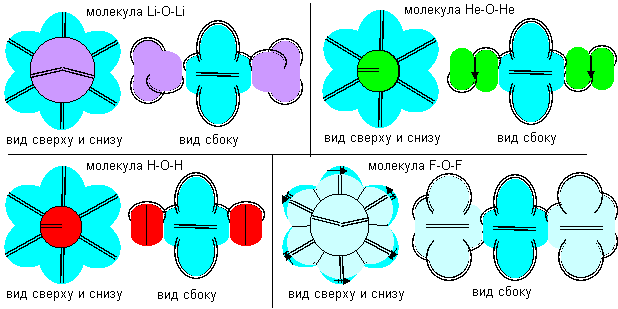
Рисунок 5. Примеры соединений атомов кислорода третьей конфигурации
Описание соединений атомов восьмой конфигурации затрудняется в связи со сложностью трехмерного изображения таких соединений с разных точек зрения. Достаточно показать соединение с атомами водорода.
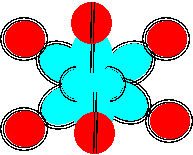
Рисунок 6. Соединение с водородом атома кислорода восьмой конфигурации
Владимир Яковлев, lun1@list.ru , http://logicphysic.narod.ru , апрель 2010 года